想看真實案例?10秒註冊
加入平台
返回文章列表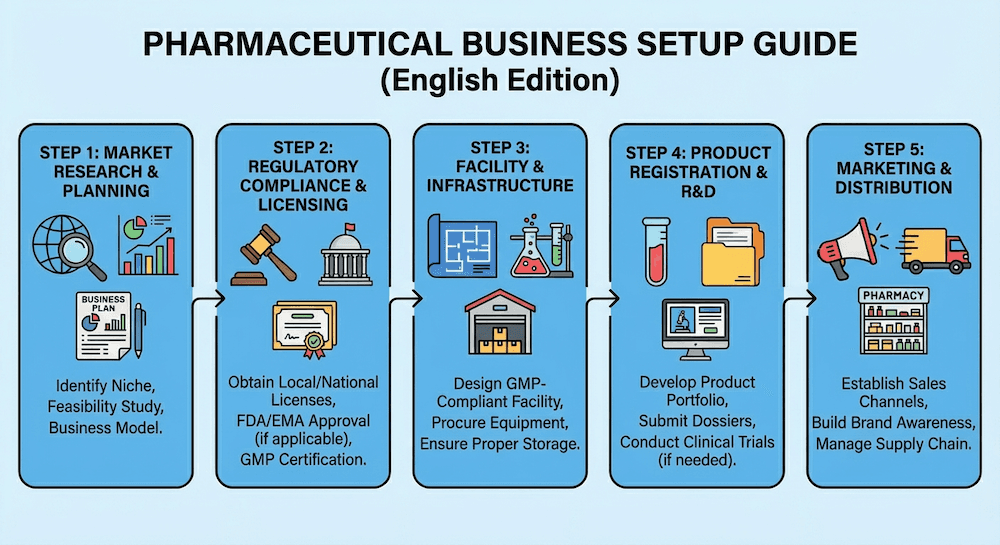

其他
2024年10月15日
約5分鐘

在香港設立您的藥業企業 (Pharmaceutical Business Setup)
在香港建立藥業企業需要仔細規劃、法規合規和戰略決策。這份全面指南涵蓋了藥業企業設立的所有方面。
業務規劃和結構
商業實體類型
選擇適當的業務結構:
- 有限公司 (Limited Company)(藥業企業最常見)
- 獨資企業 (Sole Proprietorship)
- 合夥企業 (Partnership)
- 海外公司分公司 (Branch Office)
主要考慮因素:
- 責任保護 (Liability Protection)
- 稅務影響 (Tax Implications)
- 法規要求 (Regulatory Requirements)
- 投資和資金需求 (Investment and Funding Needs)
- 未來擴展計劃 (Future Expansion Plans)
法規牌照要求
藥業企業核心牌照
批發商牌照 (Wholesale Dealer License, WDL)
用於:
- 藥品批發分銷 (Wholesale Distribution of Pharmaceutical Products)
- 進出口活動 (Import and Export Activities)
- 藥品儲存和處理 (Storage and Handling of Medicines)
- 供應給持牌場所 (Supply to Licensed Premises)
製造商牌照 (Manufacturing License)
用於:
- 本地藥品製造 (Local Pharmaceutical Manufacturing)
- 良好製造規範合規 (Good Manufacturing Practice, GMP Compliance)
- 質量控制實驗室 (Quality Control Laboratories)
- 包裝和標籤作業 (Packaging and Labeling Operations)
零售牌照
- 註冊毒藥銷售商 (Authorized Seller of Poisons, ASP) 用於全面藥房服務
- 表列毒藥銷售商 (Listed Seller of Poisons, LSP) 用於非處方藥物
專業牌照
- 危險藥物牌照 (Dangerous Drug License)(用於受管制物質)
- 抗生素許可證 (Antibiotics Permit)(用於抗生素產品)
- 臨床試驗證書 (Clinical Trial Certificate)(用於研究活動)
場所和設施要求
批發和儲存設施
要求包括:
- 足夠的儲存空間和容量
- 溫度和濕度控制系統 (Temperature and Humidity Control Systems)
- 安全措施和進入控制 (Security Measures and Access Controls)
- 不同產品類型的隔離區域 (Segregation Areas)
- 質量控制和檢疫區域 (Quality Control and Quarantine Areas)
良好分銷規範合規 (Good Distribution Practice, GDP Compliance)
- 書面程序和文件 (Written Procedures and Documentation)
- 員工培訓和能力 (Staff Training and Competency)
- 溫度監測和驗證 (Temperature Monitoring and Validation)
- 可追溯性和召回程序 (Traceability and Recall Procedures)
- 定期審計和審查 (Regular Audits and Reviews)
製造設施(如適用)
- 良好製造規範合規 (Good Manufacturing Practice, GMP Compliance)
- 經驗證的製造過程 (Validated Manufacturing Processes)
- 質量控制實驗室 (Quality Control Laboratories)
- 環境監測 (Environmental Monitoring)
- 廢物管理系統 (Waste Management Systems)
人員配置
關鍵人員要求
- 負責人 (Responsible Person, RP) 具有適當資格
- 註冊藥劑師 (Registered Pharmacist)(用於 ASP 營運)
- 質量保證人員 (Quality Assurance Personnel)
- 法規事務專家 (Regulatory Affairs Specialists)
資格和培訓
- 相關藥學教育和經驗
- 香港註冊和牌照 (Hong Kong Registration and Licensing)
- 持續專業發展 (Ongoing Professional Development)
- 合規培訓和能力評估 (Compliance Training and Competency Assessment)
質量管理系統
ISO 標準實施
考慮實施:
- ISO 9001(質量管理)
- ISO 13485(醫療器械質量管理)
- ISO 14001(環境管理)
- ISO 45001(職業健康和安全)
文件要求
- 質量手冊和程序 (Quality Manual and Procedures)
- 標準操作程序 (Standard Operating Procedures, SOPs)
- 批次生產記錄 (Batch Production Records)
- 質量控制記錄 (Quality Control Records)
- 變更控制程序 (Change Control Procedures)
- 偏差和 CAPA 系統 (Deviation and CAPA Systems)
法規合規框架
藥物警戒系統
建立系統用於:
- 不良事件監測和報告 (Adverse Event Monitoring and Reporting)
- 信號檢測和評估 (Signal Detection and Evaluation)
- 風險評估和管理 (Risk Assessment and Management)
- 安全資料庫維護 (Safety Database Maintenance)
產品註冊和生命週期管理
- 初始產品註冊 (Initial Product Registration)
- 變更申請 (Variation Applications)
- 續期程序 (Renewal Procedures)
- 上市後監察 (Post-Market Surveillance)
進出口合規
- 牌照申請和續期 (License Applications and Renewals)
- 文件要求 (Documentation Requirements)
- 海關程序 (Customs Procedures)
- 國際協調 (International Harmonization)
財務考量
啟動成本
預算包括:
- 商業註冊和牌照費用
- 場所設置和設備 (Premises Setup and Equipment)
- 員工招聘和培訓 (Staff Recruitment and Training)
- 專業服務和諮詢 (Professional Services and Consultancy)
- 營運資金和庫存 (Working Capital and Inventory)
持續營運成本
- 牌照續期費用 (License Renewal Fees)
- 設施維護和公用事業 (Facility Maintenance and Utilities)
- 員工薪金和福利 (Staff Salaries and Benefits)
- 專業賠償保險 (Professional Indemnity Insurance)
- 法規合規和審計 (Regulatory Compliance and Auditing)
資金選擇
- 個人投資 (Personal Investment)
- 銀行貸款和融資 (Bank Loans and Financing)
- 風險投資和私募股權 (Venture Capital and Private Equity)
- 政府補助和激勵 (Government Grants and Incentives)
- 戰略夥伴關係 (Strategic Partnerships)
技術和 IT 基礎設施
基本系統
- 庫存管理系統 (Inventory Management Systems)
- 客戶關係管理 (Customer Relationship Management, CRM)
- 企業資源規劃 (Enterprise Resource Planning, ERP)
- 文件管理系統 (Document Management Systems)
- 合規追蹤系統 (Compliance Tracking Systems)
數據保護和安全
- 個人數據私隱合規 (Personal Data Privacy Compliance)
- 網絡安全措施 (Cybersecurity Measures)
- 備份和災難恢復 (Backup and Disaster Recovery)
- 進入控制和審計追蹤 (Access Controls and Audit Trails)
市場進入策略
目標市場分析
- 醫療機構和醫院 (Healthcare Institutions and Hospitals)
- 零售藥房和診所 (Retail Pharmacies and Clinics)
- 政府採購 (Government Procurement)
- 出口市場和國際分銷 (Export Markets and International Distribution)
合作機會
- 本地分銷商和代理 (Local Distributors and Agents)
- 醫療保健提供者 (Healthcare Providers)
- 研究機構 (Research Institutions)
- 國際製藥公司 (International Pharmaceutical Companies)
常見挑戰和解決方案
法規複雜性
- 挑戰:導航複雜的牌照要求
- 解決方案:專業法規諮詢 (Professional Regulatory Consulting)
競爭和市場准入
- 挑戰:既定的市場參與者
- 解決方案:差異化和細分定位 (Differentiation and Niche Positioning)
人才獲取
- 挑戰:熟練的藥學專業人員
- 解決方案:有競爭力的套餐和發展計劃
技術實施
- 挑戰:系統整合和驗證 (System Integration and Validation)
- 解決方案:分階段實施和專家支持
成功最佳實踐
1. 法規卓越
- 跟上法規變更
- 投資於合規系統和培訓
- 與當局保持良好關係
- 為檢查和審計做準備 (Prepare for Inspections and Audits)
2. 質量焦點
- 實施強大的質量管理系統
- 定期內部審計和審查
- 持續改進文化 (Continuous Improvement Culture)
- 客戶滿意度監測 (Customer Satisfaction Monitoring)
3. 戰略規劃
- 明確的業務目標和里程碑
- 定期策略審查和更新 (Regular Strategy Reviews and Updates)
- 風險評估和緩解 (Risk Assessment and Mitigation)
- 繼任規劃和連續性 (Succession Planning and Continuity)
4. 專業網絡
- 行業協會和商會 (Industry Associations and Chambers)
- 專業發展小組 (Professional Development Groups)
- 法規論壇和會議 (Regulatory Forums and Conferences)
- 國際夥伴關係 (International Partnerships)
未來機遇
數字健康和創新
- 遠程醫療和數字療法 (Telemedicine and Digital Therapeutics)
- 人工智能和機器學習 (Artificial Intelligence and Machine Learning)
- 區塊鏈和供應鏈透明度 (Blockchain and Supply Chain Transparency)
- 個性化醫學和基因組學 (Personalized Medicine and Genomics)
區域擴張
- 大灣區一體化 (Greater Bay Area Integration)
- 東盟市場機會 (ASEAN Market Opportunities)
- 一帶一路倡議參與 (Belt and Road Initiative Participation)
- 跨境電子商務 (Cross-Border E-commerce)
結論
在香港設立藥業企業需要全面規劃、法規專業知識和戰略執行。成功取決於了解本地要求、建立強大的營運能力和維持合規卓越。
如需藥業企業設立的專業協助,請聯絡 ElendiLabs 獲得全面諮詢和支持服務。
無與倫比的價格
香港醫療器械註冊的透明且具競爭力的收費。
ElendiLabs 法規事務團隊
經驗證的 RA 顧問
100+產品成功註冊於全球市場。快速獲取超值報價與專家解答。
有任何問題?
我們會親自跟進回覆您。
100% 回覆率 • 7個工作天內回覆
重要免責聲明